INTRODUÇÃO
Os
cientistas dizem que matéria é tudo aquilo que existe e
que ocupa um lugar no espaço e que ela é constituiente
de todas os maetrias existentes. Que é sempre constituída
por particulas com massa não-nula ( como os átomos e,
em escala menor, os prótons, nêutrons e elétrons
). Ainda pode-se interpretala como energia vibratória de
baixa frequência.
De acordo com a pressão e temperatura a que um corpo está submetido, a matéria pode-se encontrar em três estados diferentes: sólido, líquido e gasoso. O que define cada estado físico é a proximidade e a intensidade da interação entre as partículas constituintes de uma substância.
-
ESTADO SÓLIDO
No estado sólido os constituintes atômicos encontram-se ligados fortemente, o que determina forma e volume fixos e pequena vibração em torno da posição de equilíbrio. A distância entre os átomos também é muito pequena. Como exemplo desse estado da matéria temos o gelo, que representa como as forças de atração entre os átomos são fortes, já que para que ocorra alteração da forma do corpo é necessário variar temperatura e pressão sobre o mesmo. A forma dos sólidos é definida, não dependendo do meio em que estão inseridas.
-
ESTADO LÍQUIDO
No estado líquido os grupamentos atômicos de uma substância encontram-se dispersos, de forma menos ordenada se comparados aos do estado sólido pois possuem maior movimentação e menor força de atração entre si. Conseqüentemente a distância entre os átomos é maior, o que permite que um maior volume seja ocupado. Substâncias líquidas têm a característica de tomar a forma do recipiente em que estão contidas e podemos tomar como exemplo a água contida em um copo.
-
ESTADO GASOSO
Na fase gasosa as substâncias são formadas por átomos altamente desordenados e que possuem alta energia de vibração, baixa intensidade de atração e distância interatômica pequena. O volume e forma dos gases não são definidos, pois ocupam todo espaço que se encontram e os átomos se movimentam livremente em todas as direções.

Existem processos responsáveis pela mudança do estado físico das substãncias, os quais estão representados na figura abaixo.
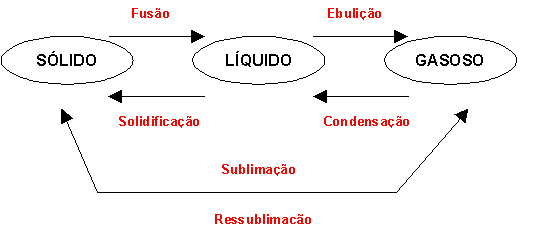
Nos processos de fusão, ebulição e sublimação ocorre consumo de energia térmica. Ao contrário, nos processos de condensação, solidificação e ressublimação, ocorre perda de calor.
Em laboratório e com a ajuda de professores é possível realizar esses processos de maneira simples, utilizando o recurso de mais fácil obtenção, a água em seus três fases: gelo (sólido), líquida e vapor (gasoso).